La tabla periódica

Utiliza el código QR para interactuar con la tabla periódica o presiona aquí
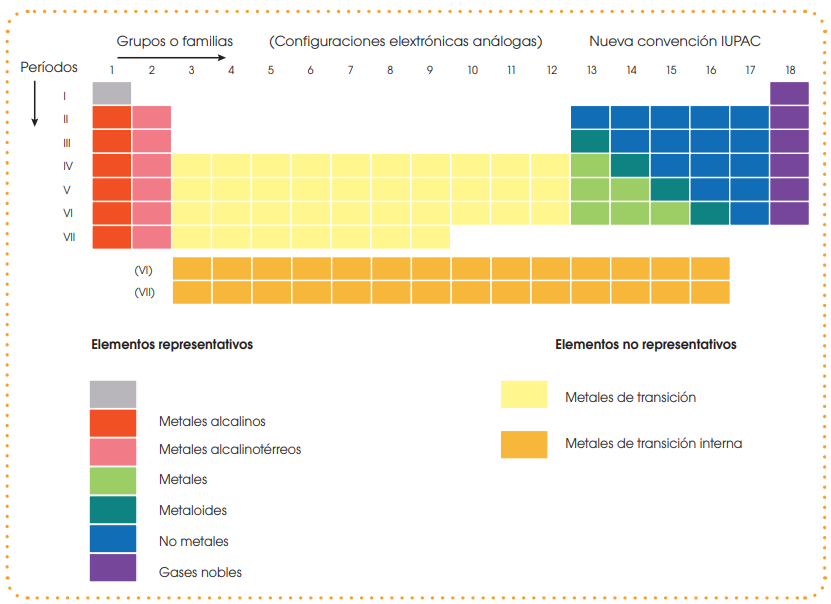
La tabla periódica muestra de una forma sencilla y visual, además de algunas de las características propias de cada elemento, la variación de la estructura interna y de propiedades de los distintos elementos a lo largo de ella.

La disposición de los elementos en el sistema periódico actual no se produce al azar, si no que responde a la llamada ley periódica que se enuncia así:


La tabla periódica actual consiste en un cuadro de doble entrada en el que los elementos están agrupados en siete periodos (filas) y dieciocho grupos (columnas).





TABLA PERIÓDICA
ESTRUCTURA ELECTRÓNICA
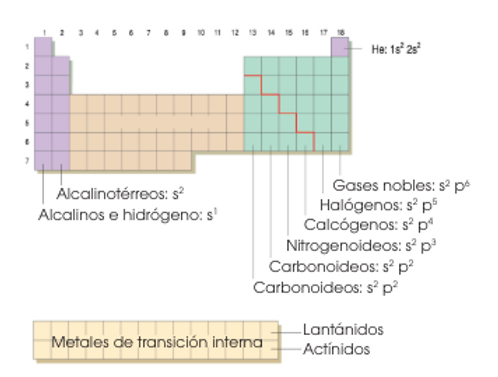
Al comparar la configuración electrónica de los elementos con su situación en la tabla periódica, observamos que:
-
Todos los elementos de un mismo período tienen el mismo número de niveles electrónicos, completos o no. Este número coincide con el número del período (tabla).
-
Los elementos de un mismo grupo presentan la misma estructura electrónica en su nivel más externo, o capa de valencia.
Presiona aquí para jugar




Elementos Representativos
-
Los metales alcalinos: Corresponden al grupo o familia 1A de la tabla periódica.
-
Los metales alcalinos térreos: Son metales del grupo o familia 2A.
-
Los metales térreos: Lo forman metales del grupo o familia 3A de la tabla periódica.
-
Grupo 4A o carbonoides: Forman el grupo 14 de la tabla periódica.
-
Grupo 5A o nitrogenoides: Nitrógeno, fósforo, arsénico, antimonio, bismuto y ununpentio.
-
Grupo 6A o anfígenos: Oxígeno, azufre, selenio, teluro, polonio y ununhexio.
-
Grupo 7A o halógenos: Son no metales como el flúor, cloro, bromo, yodo, ástato y ununseptio.
-
Grupo 8A o gases nobles: Son el helio, neón, argón, criptón, xenón y radón.Los grupos o familias B corresponden a los elementos de transición.