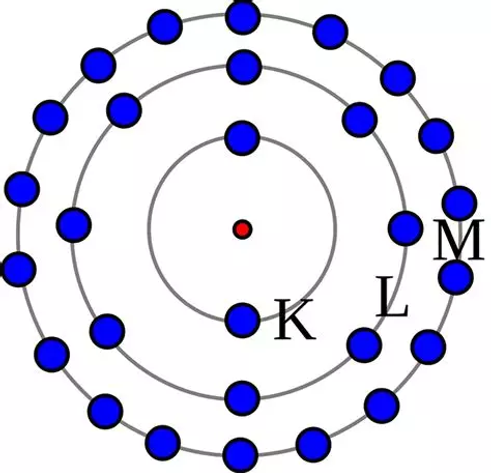
El modelo planetario de Bohr
En 1913, el físico danés Niels Bohr propuso un nuevo modeloatómico. Para Bohr, los electrones giraban en torno al núcleoen órbitas circulares de radios deinidos, pero no en todaslas órbitas, pues para él existían órbitas permitidas y otrasprohibidas.
En cada una de estas órbitas solo puede haber un núme-ro dado de electrones, con una energía determinada. Paraque un electrón cambie de órbita, es necesario modiicar suenergía en una cantidad determinada.
Hacia 1925, nuevos avances, tanto experimentales comoteóricos, obligaron a proponer un nuevo modelo: el mode-lo atómico de orbitales. A partir de los trabajos de cientíi-cos como Max Planck, Louis De Broglie, Werner Heisenberg,Erwin Schrödinger y otros, se ha establecido el modelo ató-mico actual.
En este modelo, los electrones no describen órbitas deinidasen torno al núcleo, como había supuesto Rutherford, sinoque se encuentran distribuidos ocupando orbitales.Este modelo es acertado a nivel atómico y molecular (molé-culas, átomos y partículas subatómicas).